Incontinencia Urinaria de Esfuerzo: Tratamiento con Inyección de Plasma Rico en Plaquetas y Colocación de Hilos de Polidioxanona – Un Estudio Piloto
Artículo Publicado en The American Journal of Cosmetic Surgery.
Por: Ariel Luksenburg, MD , Juan J. Barcia, MD, Roberto Sergio, MD, Santiago Fernandez, MD, Marco A. Pelosi II, MD, and Marco A. Pelosi III, MD.
Resumen:
La incontinencia urinaria por esfuerzo es un importante problema clínico que afecta a millones de mujeres en todo el mundo. El objetivo de este artículo fue evaluar un procedimiento mínimamente invasivo como tratamiento alternativo para la incontinencia urinaria por esfuerzo leve en mujeres, utilizando inyecciones de plasma rico en plaquetas (PRP) y hilos de polidioxanona (PDO). Un total de 23 pacientes con incontinencia urinaria leve, con una edad media de 46 años, fueron evaluadas mediante historia detallada, examen físico, diario urinario, análisis de laboratorio completo, ultrasonografía, estudios urodinámicos y completando el Cuestionario de Consulta Internacional sobre Incontinencia – Formulario Corto de Incontinencia Urinaria (ICIQ-UI SF, por sus siglas en inglés). Bajo anestesia local, se inyectó PRP a través de la pared vaginal anterior, y se colocaron hilos de PDO en espacios parauretrales, suburetrales y uretrovaginales laterales, utilizando instrumentos desarrollados para un desempeño seguro y efectivo. Las pacientes fueron analizadas a las 1, 2, 4 y 8 semanas, y a los 6 meses después del tratamiento. Un total de 10 pacientes fueron biopsiadas antes de la operación y 60 días después del tratamiento. Los síntomas y la puntuación de ICIQ-UI SF mejoraron significativamente. Los estudios urodinámicos posoperatorios fueron normales en todos los casos. Las biopsias después del tratamiento mostraron una malla de tejido conectivo denso tridimensional. No se observaron complicaciones ni efectos adversos. Todas las pacientes declararon estar satisfechas con los resultados, se someterían al procedimiento nuevamente y lo recomendarían. La técnica mínimamente invasiva presentada aquí resulta en el fortalecimiento de los espacios parauretrales, suburetrales y uretrovaginales laterales, y de la mucosa de la pared vaginal anterior. La combinación de las inyecciones de PRP y la colocación de hilos de PDO crea una estructura similar a una malla fibrosa y absorbible, con el objetivo de aumentar la resistencia uretral, de modo que bajo esfuerzo la presión intravesical no supere la presión uretral. Estos resultados sugieren que el procedimiento es seguro y una alternativa rentable en pacientes con incontinencia urinaria leve, reduciendo la necesidad de procedimientos quirúrgicos invasivos. Se necesitan estudios más amplios para confirmar los resultados de este estudio.
Introducción
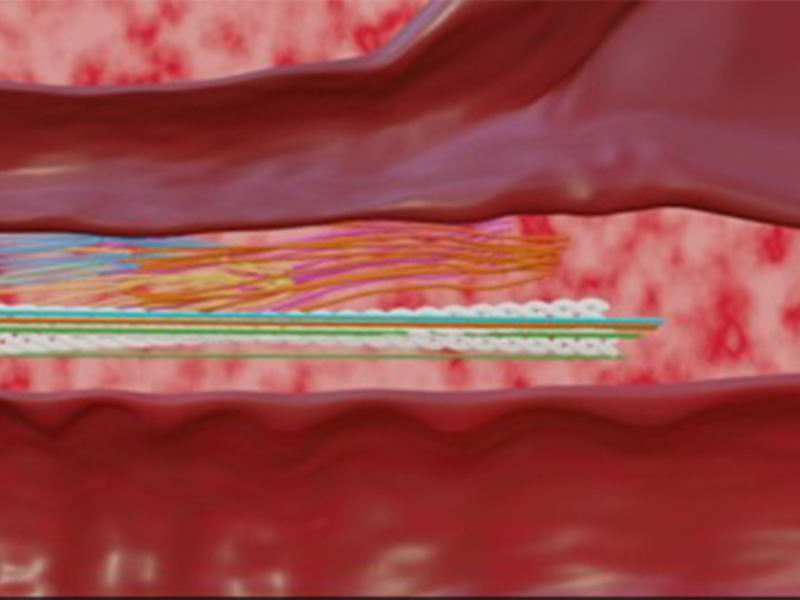
La incontinencia urinaria por esfuerzo es un importante problema clínico que afecta a millones de mujeres en todo el mundo. La pérdida de orina está relacionada con un aumento de la presión intraabdominal y puede tener una causa anatómica, debido a la hiperactividad uretral en la que los elementos de retención uretral están debilitados o dañados, o debido a una deficiencia funcional intrínseca del esfínter. Los tratamientos actuales pueden ser quirúrgicos o no quirúrgicos. Todos ellos tienen tasas de éxito variables y posibles complicaciones. Además, los tratamientos quirúrgicos tienen un costo relativamente alto. Los autores han desarrollado un tratamiento mínimamente invasivo para pacientes que sufren de incontinencia urinaria leve con el objetivo de fortalecer el suelo pélvico, utilizando una combinación de inyecciones de plasma rico en plaquetas (PRP) a través de la mucosa de la pared vaginal anterior, y la colocación de hilos de polidioxanona en los espacios parauretrales, suburetrales y uretrovaginales laterales, para crear un soporte absorbible similar a una malla.
La malla creada por las inyecciones de PRP y los hilos de polidioxanona tiene como objetivo aumentar la resistencia uretral con la reducción de la hiperactividad uretral, para que la presión intravesical no supere la presión uretral durante el estrés físico.
El objetivo de este procedimiento es lograr la remisión de la incontinencia urinaria. Presentamos los resultados de nuestro estudio piloto en 23 pacientes que sufren de incontinencia urinaria leve.
Materiales y método
Tratamos a un total de 23 pacientes con una mediana de edad de 52 años (rango de 45 a 66), con incontinencia urinaria leve (grado 1 o de leve severidad, definido como pérdida de orina con aumentos súbitos de la presión abdominal: por ejemplo, tos, estornudos o risa). El índice de severidad se basa en la información sobre la frecuencia (cuatro niveles) y la cantidad de pérdida (dos o tres niveles). Al multiplicar, se alcanza un valor de índice (1-8 o 1-12). Este valor de índice se categoriza aún más en un índice de severidad de tres o cuatro niveles. Las preguntas utilizadas para evaluar el grado de incontinencia urinaria en mujeres fueron las siguientes:
¿Con qué frecuencia experimenta pérdida de orina?
- Menos de una vez al mes
- Algunas veces al mes
- Algunas veces a la semana
- Todos los días y/o noche
¿Cuánta orina pierde cada vez?
- Gotas
- Salpicaduras pequeñas
- Más
El índice de severidad se crea multiplicando los resultados de las preguntas 1 y 2. En el índice de severidad de tres niveles, las respuestas a la segunda pregunta se agregan primero en gotas (1) y más (2), y luego se multiplican con la frecuencia, dando como resultado los siguientes valores de índice (1-8):
1-2 → leve
3-4 → moderado
6-8 → severo
El índice de severidad de cuatro niveles se basa en los siguientes valores de índice (1-12):
1-2 → leve
3-6 → moderado
8-9 → severo
12 → muy severo
Todas las pacientes estaban en período menopáusico y todas con hasta 2 partos. Después de una historia detallada y un examen físico, las pacientes fueron evaluadas con un diario urinario de 3 días, análisis de orina completo, cultivo de orina, ICIQ-SF (Cuestionario de Consulta Internacional sobre Incontinencia – Formulario Corto), ultrasonografía (para confirmar la hiperactividad uretral y excluir patologías incidentales), pruebas bioquímicas de rutina y estudios urodinámicos (uroflujometría libre, cistometrograma, presión cistomanométrica, flujo de presión, presión del detrusor y residuo de orina).
Se excluyeron del estudio a las pacientes que habían sido sometidas a cirugía previa de incontinencia, cirugía uretral o de la pared vaginal anterior, cesárea, inyecciones de relleno parauretrales y suburetrales, prolapso uterino o rectal concomitante, y pacientes con infecciones del tracto urinario o trastornos hemorrágicos.
Una semana antes del procedimiento, se realizó un cultivo de orina para confirmar la ausencia de infección urinaria. Si era posible, se suspendieron los medicamentos anticoagulantes orales 24 horas antes.
Todos los aspectos de nuestro protocolo se llevaron a cabo en nuestra clínica de práctica privada y se realizaron de acuerdo con las pautas aprobadas por el Ministerio de Salud Pública (Uruguay) relacionadas con los estándares éticos del Comité de Investigación que Involucra a Seres Humanos y con la Declaración de Helsinki.
Cada paciente firmó un consentimiento informado después de una explicación detallada del proceso de tratamiento, los posibles beneficios y riesgos, las posibles complicaciones, la inclusión de los resultados en un artículo y el hecho de que este era un tratamiento nuevo. Todas las pacientes recibieron 2 tratamientos separados por 30 días. Cada paciente fue monitoreada a los 7, 15, 30 y 60 días después del tratamiento. Los estudios urodinámicos se repitieron 6 meses después.
Para considerar la mejora de la incontinencia urinaria, las pacientes necesitaban historial y registros diarios con una reducción en los índices de severidad, estudios urodinámicos cercanos a la normalidad, y evidencia ultrasonográfica de reducción de la hiperactividad uretral.
Para estudios comparativos, se realizaron biopsias punzantes parauretrales en 10 pacientes antes del tratamiento y 60 días después de completar el tratamiento. Cada paciente biopsiada firmó un consentimiento informado aprobando el procedimiento de biopsia. Las muestras se fijaron en formol tamponado al 10% y luego se procesaron (desecación, inclusión en parafina y corte de 7 micras). Se realizaron tinciones con Hematoxilina-Eosina, tricrómico de Masson, reactivos de ácido períódico-Schiff (PAS) e impregnación de plata para reticulina. Se analizó la calidad y cantidad de colágeno, evidencia de elementos inflamatorios (edema, dilatación vascular, exudado celular), densidad vascular, estado de la matriz intercelular y celularidad, y subtipos de colágeno.

Las pacientes fueron tratados de manera ambulatoria
Las pacientes fueron colocadas en posición de litotomía dorsal. Aproximadamente 25 minutos antes del procedimiento se aplicó un anestésico tópico en la pared vaginal anterior que cubre el meato uretral, áreas parauretrales, suburetrales y uretrovaginales laterales. El tratamiento consta de 2 pasos, que duran aproximadamente 40 minutos: primero, la inyección de PRP en la pared vaginal anterior seguida de la inserción de hilos de polidioxanona en los espacios parauretrales, suburetrales y uretrovaginales laterales. Mientras se realizaban las maniobras y 24 horas después de terminar, las pacientes fueron evaluadas por dolor utilizando la escala analógica visual (VAS) y la escala de valoración numérica (NRS) para evaluar la intensidad del dolor.
Paso 1: Inyecciones de PRP en la Pared Vaginal Anterior.
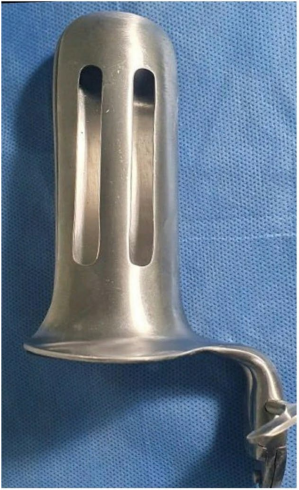
Se extraen 8 mL de sangre utilizando tubos de 4 mL con citrato de sodio al 3.8% (GyCO. Deltalab. España). A continuación, se realiza una centrifugación durante 8 minutos a 1800 rpm. El plasma separado se extrae utilizando jeringas de 1 mm. Por cada jeringa de 1 mm, se mezclan 0.9 mL de plasma con 0.1 mL de cloruro de calcio (GyCO. Deltalab. España). Las jeringas de 1 mm se conectan a agujas de 30G × 1⁄2 (13 mm). Para facilitar las inyecciones transvaginales del PRP en la pared vaginal anterior, los autores han desarrollado un nuevo espéculo fenestrado (Figura 1). El espéculo fenestrado está hecho de acero inoxidable, tiene 2 fenestraciones laterales y longitudinales paralelas de 7 mm de ancho y 65 mm de largo. Separando las 2 fenestraciones, hay un puente central y longitudinal sólido. La función del puente es proporcionar estabilidad al espéculo, protección mecánica de la uretra y guiar la colocación de las inyecciones de PRP y los hilos de PDO. Para indicar la posición del meato urinario, hay una marca de referencia en el punto de las 12 en punto. Después de colocar y posicionar el espéculo, se inyecta el PRP en la pared vaginal anterior a través de las 2 fenestraciones del espéculo. De atrás hacia adelante. Las infiltraciones de PRP se realizan inyectando solo el bisel de la aguja en la mucosa vaginal con un ángulo de 45 grados. Aproximadamente se coloca 0.2 mL de PRP con cada inyección. Se utilizan un promedio de 10 inyecciones de PRP por lado.
Paso 2: Colocación de Hilos de PDO (Polidioxanona)
Los hilos de polidioxanona son esterilizados, compatibles con los tejidos y se reabsorben en 6 meses después de la colocación. El hilo de PDO tiene una longitud de 45 mm, un grosor de 0.15 mm (4-0) y una configuración de tornillo de corcho montado en una aguja de 25G × 30 mm (GyCO International. Shanxian Runte Medical International, Ltd., China). Los hilos de PDO se colocarán secuencialmente en las áreas parauretrales, uretrovaginales laterales y suburetrales. El acceso de los hilos de PDO al espacio uretrovaginal vaginal se monitorizó y realizó bajo visión ecográfica.
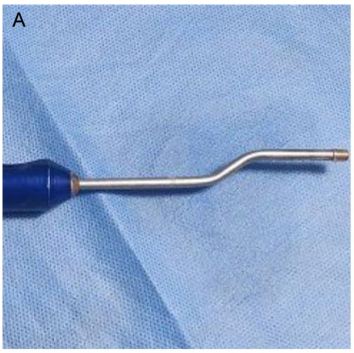

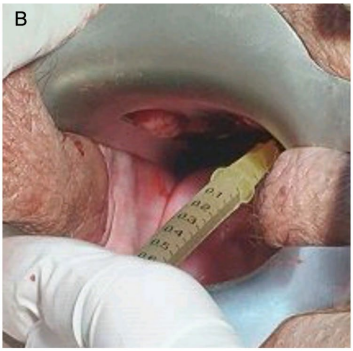
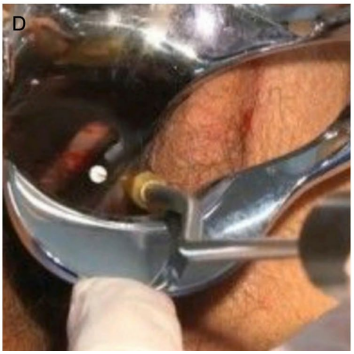
Colocación de los Hilos de PDO en las Áreas Parauretrales
Para facilitar la colocación de los hilos de PDO, los autores han desarrollado un instrumento llamado Bayoneta 1. Actúa como una extensión de la mano del operador, permitiendo la inserción fácil de los hilos en la pared vaginal anterior. El mango de la bayoneta mide 10 cm de largo y está unido a una varilla de metal de 13.5 cm de largo. En su extremo, la varilla tiene una forma de S con un ángulo de 30°. Tiene un indicador de presión que se adapta al cubo de la aguja con el hilo de PDO. Con el espéculo fenestrado en su lugar mostrando la marca del meato uretral a las 12 en punto, la Bayoneta 1 con el hilo de PDO adjunto se guía hacia el cuarto anterior de una de las ventanas fenestradas. Los hilos se insertan en la pared vaginal de atrás hacia adelante, con un ángulo de 30°. Una vez que la aguja ha alcanzado una profundidad de 1 cm, se avanza recta hasta que esté completamente insertada. Esta maniobra se realiza con guía ultrasonográfica. La Bayoneta 1 con el cubo de la aguja se retira, dejando el hilo de PDO libre en el área parauretral, paralelo a la uretra. Luego, el procedimiento se repite en el mismo lado otras 2 veces. Se repite el mismo procedimiento en el lado contralateral.
Colocación de los Hilos de PDO en los Espacios Uretrovaginales Laterales
Para colocar hilos adicionales de PDO en el espacio uretrovaginal entre el área parauretral y la rama isquiopúbica ipsilateral, el espéculo se gira hacia afuera 1 cm, y se colocan 2 hilos de PDO a través de la ventana fenestrada. En algunas pacientes con espacios uretrovaginales laterales amplios, puede ser necesario colocar hilos de PDO adicionales para alcanzar la rama isquiopúbica. Estos hilos adicionales se colocan después de girar el espéculo hacia afuera 1 cm desde la posición anterior, y luego se colocan 2 o más hilos de PDO a través de la ventana fenestrada. El mismo procedimiento se repite en el lado contralateral.
Colocación de los Hilos de PDO en el Espacio Suburetral
Para facilitar la colocación de los hilos en el espacio suburetral, los autores han diseñado un instrumento llamado Bayoneta 2. El instrumento tiene un mango de 10 cm de largo unido a una varilla de acero inoxidable de 13.5 cm de largo con una forma de S en su extremo, con un ángulo de 29°. Al final de la sección recta de la varilla y 1.5 cm antes del inicio de la sección en forma de S, hay una estructura en forma de U con 2 brazos de 8 mm de largo, paralelos a la varilla central. En el extremo de los 2 brazos, hay 2 indicadores de presión, que se adaptarán al cubo de las agujas con los hilos de PDO. Un catéter Foley estándar se transecta 4 cm desde su extremo y se coloca para cubrir completamente el extremo romo de la varilla central. La varilla central con su catéter de cobertura es 2 cm más larga y 1.5 cm más alta que el extremo distal de las agujas. La apariencia final del instrumento se asemeja a un "tridente". Con la paciente en posición de litotomía semisentada, se retira el espéculo vaginal fenestrado, y bajo condiciones estériles se lubrican la uretra y el catéter con gel (clorhidrato de lidocaína al 2%). Luego, se introduce la varilla central en la uretra aproximadamente 2 cm y luego se eleva ligeramente hacia arriba la uretra, antes de que las agujas con los hilos de PDO hagan contacto con la mucosa vaginal. Esta maniobra protege la uretra de las agujas que se colocarán debajo de la uretra. En este punto, se introduce completamente la Bayoneta 2. Luego se retira la bayoneta y se colocan los 2 hilos de PDO liberados en el espacio suburetral. La colocación de los hilos de PDO en los espacios suburetrales, parauretrales y uretrovaginales laterales ha sido completada, creando una estructura similar a una malla que cubre el espacio uretrovaginal desde la rama isquiopúbica derecha hasta la izquierda.
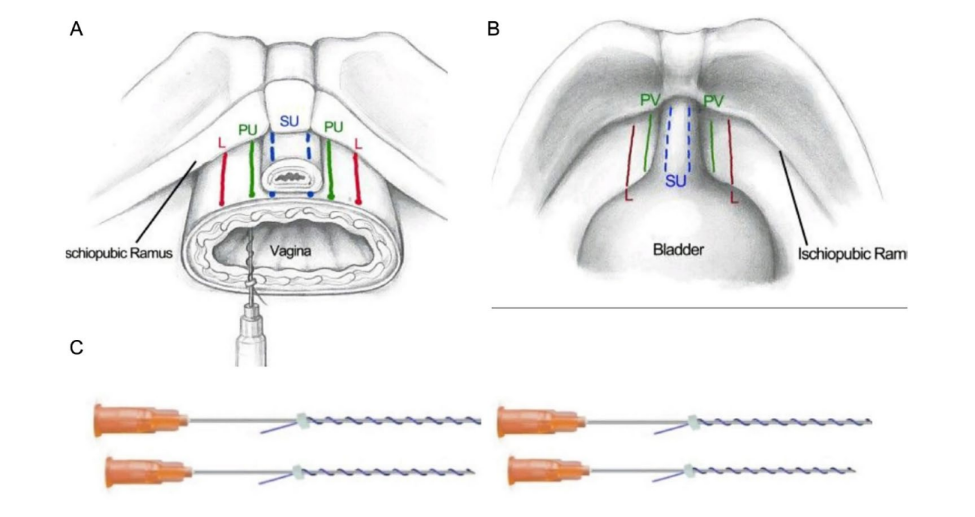
Resultados
Cuando se evaluaron a las pacientes de acuerdo con el diagnóstico, empleando los mismos cuestionarios y registros diarios, los síntomas de incontinencia urinaria mejoraron en un 100%. Solo 1 paciente (4.34%) reportó recaída de los síntomas a las 4 semanas después del tratamiento. La mejora subjetiva de los síntomas apareció en un promedio de 5 días después del tratamiento inicial. A las 4 semanas y 6 meses después del tratamiento, las puntuaciones de ICIQ-UI SF mejoraron significativamente con respecto a los niveles previos al tratamiento. Antes del tratamiento, la puntuación media de ICIQ-UI SF fue de 12.5 (10-15 puntos), al final de la primera semana la puntuación media fue de 3.5 (1-5 puntos) y a las 4 semanas y 6 meses después del tratamiento, la puntuación fue de 0. La evaluación urodinámica preoperatoria demostró incontinencia urinaria leve objetiva en todos los casos. Después del tratamiento, los estudios urodinámicos fueron normales en todas las pacientes. No hubo efectos adversos ni complicaciones asociadas con los procedimientos. La evaluación del dolor fue negativa, ninguna de las pacientes se quejó de dolor durante el procedimiento o hasta 24 horas después del mismo. Inmediatamente después del examen clínico después del tratamiento, no se observaron alteraciones funcionales ni cicatrices hipertróficas. Las biopsias previas al tratamiento mostraron tejido conectivo laxo, con escaso tejido adiposo en forma de islotes, y una ligera congestión vascular. Las biopsias posteriores al tratamiento revelaron la presencia de cavidades en el tejido conectivo subepitelial, resultado de los hilos de PDO reabsorbidos. Estas cavidades estaban rodeadas por anillos o bandas de tejido conectivo denso que alcanzaban hasta 80 micrones de ancho, que se interconectaban creando una red tridimensional centrada por los caminos de los hilos. Hubo un aumento leve a moderado en la celularidad de los fibroblastos/mioblastos, la densidad vascular y el colágeno tipo III. No se observó aumento en las fibras elásticas ni elementos inflamatorios. Las 22 pacientes con síntomas mejorados (95.66%) declararon estar satisfechas con los resultados, se someterían nuevamente al procedimiento y lo recomendarían a amigos que sufren de incontinencia urinaria leve.
Discusión
La debilidad y flacidez de los tejidos parauretrales, suburetrales y uretrovaginales laterales son dos de las principales causas responsables del desarrollo de la incontinencia urinaria por esfuerzo. La técnica mínimamente invasiva presentada aquí resulta en el fortalecimiento de los espacios parauretrales, suburetrales y uretrovaginales laterales, así como en la mucosa de la pared vaginal anterior, apuntando a las áreas por donde pasa la uretra desde la vejiga hasta el meato uretral. La combinación de las inyecciones de PRP y la colocación de hilos de PDO generan cambios seguidos por la activación de fibroblastos y miofibroblastos. El estímulo en los fibroblastos desencadena la formación de nuevas fibras de colágeno y la tensión de la pared vaginal anterior. A largo plazo, el PRP tiene un efecto modulador sobre el proceso fibrogénico, previniendo la fibrosis excesiva que podría conducir a deformaciones debido al efecto retráctil o nodulación.
Los hilos de PDO implantados en los espacios parauretrales, suburetrales y uretrovaginales laterales generan una reacción fibrogénica alrededor de los hilos tendiendo a encapsularlos. Debido a que los hilos de PDO son inertes biológicamente, no se produce una reacción de cuerpo extraño. La forma de tornillo de los hilos ayuda a crear más áreas de contacto con los tejidos huéspedes y desencadena una mayor reacción fibrosa alrededor de los hilos. Los hallazgos histológicos tras los implantes de hilos de PDO se caracterizaron por la creación de una fibrosis tridimensional alrededor de los hilos, lo que resultó en la formación de una estructura similar a una malla alrededor de ellos, y que persistió después de la reabsorción de los hilos. Nuestros hallazgos fueron similares a los cambios previamente descritos en modelos animales y tejido humano después de los implantes de hilos de PDO.
El acceso de los hilos de PDO al espacio uretrovaginal vaginal se monitorizó y realizó bajo visión y control ecográfico transperineal. Es importante destacar que la elaboración de la malla de alambre de PDO en el espacio uretrovaginal vaginal, corroborada por la sonda transvaginal del equipo de ultrasonido, proporciona seguridad y solo confirma que su elaboración se encuentra en el mismo lugar donde la malla se desliza durante el procedimiento. Para tratar la incontinencia urinaria, se utiliza la cinta obturadora transvaginal (TOT). De esta manera, accederemos a un espacio conocido, estudiado y aprobado, pero de una manera fácil, mucho menos sangrienta, mínimamente invasiva, visible y predecible, de una manera simple, efectiva, ambulatoria e indolora. Debido a que es una forma simplificada de tratamiento para la incontinencia urinaria, TOT, donde el área a la que accederemos ya ha sido estudiada y aprobada.
Una de las limitaciones de nuestro estudio es que el número de pacientes fue bajo. Se necesitan estudios aleatorizados con un mayor número de casos para confirmar los resultados positivos de este estudio piloto.
Una respuesta inmediata a las inyecciones de PRP en la mucosa vaginal anterior es el aumento del flujo sanguíneo, la permeabilidad vascular y el edema intersticial, lo que resultará en tumescencia del tejido periuretral durante aproximadamente 48 horas.
Conclusiones
Los resultados de este estudio piloto sugieren que el procedimiento es una alternativa efectiva, segura y rentable para pacientes con incontinencia urinaria leve, y puede reducir la necesidad de procedimientos quirúrgicos invasivos más agresivos. Se necesitan estudios comparativos adicionales con un mayor número de pacientes para determinar el valor del procedimiento en pacientes con incontinencia urinaria leve.
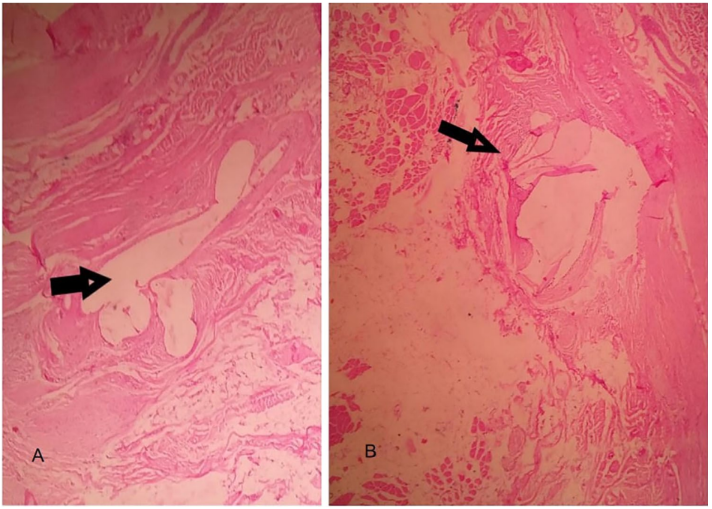
Contribuciones de los Autores
A.L. contribuyó al diseño, planificación, conducción, análisis de datos y escritura del manuscrito. J.J.B. contribuyó al diseño, planificación, análisis de datos, histopatología y escritura del manuscrito. R.S. contribuyó al diseño, planificación y conducción. S.F. contribuyó al análisis de datos urodinámicos. M.A.P. II contribuyó a la planificación, conducción, análisis de datos y escritura del manuscrito. M.A.P. III contribuyó a la planificación, conducción, análisis de datos y escritura del manuscrito.
Declaración de Conflictos de Interés
El/los autor(es) declararon los siguientes conflictos de interés potenciales con respecto a la investigación, autoría y/o publicación de este artículo: A.L., MD, es CEO de GyCO Global. El resto de los autores no tienen conflictos de interés.
Financiamiento
El/los autor(es) no recibieron apoyo financiero para la investigación, autoría y/o publicación de este artículo.
ORCID iD
Ariel Luksenburg https://orcid.org/0000-0003-0057-5472
Biografías de los Autores
Ariel Luksenburg, MD, Práctica Privada, Montevideo, Uruguay. Juan J. Barcia, MD, Dept. de Patología Quirúrgica, Hospital de Clínicas, UdelaR, Montevideo, Uruguay. Roberto Sergio, MD, Dept. de Ginecología, Hospital de Maldonado, Maldonado, Uruguay. Santiago Fernández, MD, Clínica Urodinámica, Montevideo, Uruguay. Marco A. Pelosi II, MD, Centro Médico Pelosi, Bayonne, NJ, EE. UU. Marco A. Pelosi III, MD, Centro Médico Pelosi, Bayonne, NJ, EE. UU.
Ariel Luksenburg, MD, Práctica Privada, Montevideo, Uruguay.
Juan J. Barcia, MD, Dept. de Patología Quirúrgica, Hospital de Clínicas, UdelaR, Montevideo, Uruguay.
Roberto Sergio, MD, Dept. de Ginecología, Hospital de Maldonado, Maldonado, Uruguay.
Santiago Fernández, MD, Clínica Urodinámica, Montevideo, Uruguay.
Marco A. Pelosi II, MD, Centro Médico Pelosi, Bayonne, NJ, EE. UU.
Marco A. Pelosi III, MD, Centro Médico Pelosi, Bayonne, NJ, EE. UU.